1. DİFERANSİASYON VE ANAPLAZİ
Differansiasyon (ayrımlaşma),terim olarak “bir tümörü oluşturan parankim hücrelerinin, eşdeğer matür formlarına morfolojik (mikroskopik) ve fonksiyonel olarak benzeme derecesini” belirtir.
Genel olarak benign tümörlerin hepsi iyi differansiye tümörlerdir. Yani benign tümörleri oluşturan parankim hücreleri köken aldıkları dokudaki eşdeğer, matür hücrelere hem morfolojik hem fonksiyonel olarak çok benzerler. Malign tümörlerdeki differansiasyon derecesi ise değişkendir. Bazıları iyi differansiye olabilirken, diğerleri az ya da orta derecede differansiasyon gösterebilir. Bazen hiç differansiasyon göstermeyebilirler bu tümörler için “indifferansiye ya da andifferansiye tümör” terimi kullanılır. Ayrıca, bir malign tümör iyi differansiye de olsa, hiçbir zaman differansiasyonu benign bir tümörünki kadar iyi olamaz ve bir miktar differansiasyon kaybı gösterir.
Anaplazi, bir tümörü oluşturan hücrelerdeki differansiasyonun azlığı ya da hiç bulunmamasıdır. Anaplazi terimi, anlam olarak malign tümör hücrelerinde başlangıçta var olan differansiasyonun kaybolduğunu yani tümörün “dedifferansiye” olduğunu belirtiyor gibi algılanıyorsa da, günümüzdeki bilgiler, malign tümörlerin büyük bir kısmının hemen her dokuda buluna rezerv (kök- stem) hücrelerden geliştiğini göstermektedir. Dolayısıyla, iyi differansiye malign tümörde, tümörün köken aldığı kök hücreler differansiye olmakta ve ait olduğu dokuya özgü normal hücrelere benzemeye çalışmaktadır. Öte yandan az differansiye ya da indifferansiye malign tümörlerde bu davranış ya az görülmekte ya da hiç olmamaktadır.
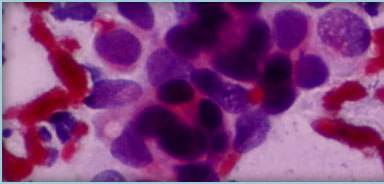
Anaplazide morfolojik değişiklikler (Hücresel atipi kriterleri)
1. Hiperkromazi: Hücre nukleusunun bol DNA içeriğine bağlı olarak Hematoksilen eozin boyası ile koyu mor boyanmasıdır.
2. Nukleus/sitoplazma oranının değişmesi: Normalde, hücrelerdeki nukleus/sitoplazma oranı 1/4 ile 1/6 arasında iken, malign tümör hücrelerinde bu oran 1/1’e yaklaşabilir.
3. Pleomorfizm: Tümörü oluşturan parankim hücreleri arasında belirgin şekil ve boyut farklılığı bulunmasıdır.
4. Belirgin nukleol varlığı.
5. Mitoz: Malign tümörleri oluşturan hücrelerde çok sayıda tipik ve atipik mitoz izlenebilir. Ancak, “tipik” mitozlar, kemik iliği ve derinin bazal tabakası gibi, çoğalmakta olan hücreler içeren normal dokularda ve “hiperplazi” durumunda da görülebilir. Malign tümöler için özellikle “atipik” mitoz varlığı önemli bir tanı kriteridir.
1. Tümör dev hücreleri, anaplastik tümörlerde görülebilir.
2. polarizasyon- organizasyon kaybı
Bir anaplazi kriteri olmamakla birlikte “nekroz” anaplastik tümörlerde sıklıkla görülebilen bir bulgudur. Bu tip tümörlerde stroma genellikle az olduğundan, parankimal tümör hücreleri için yeterli vasküler beslenme sağlanamaz ve özellikle tümörün ortasında geniş nekroz alanları ortaya çıkar.
Anaplastik tümörlerde, tümör hücrelerinin organizasyonu ortadan kalkmıştır. Elektron mikroskopik olarak iyi differansiye malign tümör hücreleri normal hücrelere çok benzerken, differansiayon azaldıkça nükleer kromatin nukleus membranında kümelenir ve spesifik organeller azalmaya başlar. Öte yandan, differansiasyon azalması ile birlikte morfoloji dışında değişen bir başka özellik tümör hücrelerinin fonksiyonel kapasitesidir. Malign tümörler ne kadar iyi differansiye ise, hücreler fonksiyonel kapasitelerini o kadar korur. Örneğin, iyi differansiye yassı hücreli karsinomda hücrelerde bol keratin yapımı, iyi differansiye hepatosellüler karsinomda da belirgin safra yapımı görülür. Endokrin organlardan gelişen benign tümörler ve iyi differansiye adenokarsinomlar sıklıkla köken aldıkları organa ait horman salgılarlar.
Anaplastik tümör hücreleri köken aldıkları doku ne olursa olsun birbirlerine benzerler ki bu duruma “biyokimyasal konverjans” denir. Ancak, bazı durumlarda, fötal yaşama ait antijen yapımı ya da endokrin dokudan köken almayan bir tümörün hormon salgılaması gibi beklenmeyen fonksiyonlar ortaya çıkabilir.
2. BÜYÜME HIZI:Bir tümörün büyümesini etkileyen faktörler: -tümör hücresinin kinetiği
-tümör anjiogenezi
Tümör Hücresi Kinetiği
1-Tümör hücrelerinin sayısının ikiye katlanması (doubling). Tümör tipine göre farklılık gösterir. Çocukluk çağı tümörlerinde 1 ay iken tükürük bezi tümöründe 1 yıldır.
2-Büyüme oranı: Prolifere hücre oranı- latent dönemde (submikroskopik dönem) hücrelerin çoğu replikatif havuzdayken klinik olarak saptanabilir durumdayken çoğu hücre nonproliferatif havuzdadırlar. Tümör hücrelerinin kohezyon kaybı kaybı sonucu dökülmeleri, beslenme yetersizliği, differansiye olmaları ya da G0 fazına dönmeleri sonucu tümör büyüdükçe hücreler giderek artan oranda çoğalma havuzundan çıkarlar. Klinik olarak saptanabilen bir tümörde hücrelerin büyük bölümü hücre siklusunun G0 fazındadır. Büyüme oranı lösemi, lenfoma gibi hızlı büyüyen tümörlerde % 20 iken meme ve kolon gibi yavaş büyüyen tümörlerde %5 lerdedir büyüme
3-Hücre üretimi-kaybı oranı: büyüme fraksiyonu. Ne kadar yüksekse tümör o kadar hızlı büyür ve kemoterapiye duyarlılık gösterir.
Ayrıca son yıllarda tümör içinde tümörü başlatma ve sürdürme kapasitesi olan ‘’kanser kök
hücreler ya da tümör başlatıcı-inisiyatör hücreler (T-IC)’’ den bahsedilmektedir ki bu hücrelerin esas
olarak tedaviye direnç ve tümörün tekrarlamasında rol oynadıkları düşünülmektedir. Ancak bugün için bu
hücrelerin akut myelositer lösemide (AML) %0.1-1 ve meme kanserinde %2 oranında bulunduğu
saptanmış, tüm tümörlerde varlıkları gösterilememiştir.
Esas olarak bir tümörde differansiasyon azaldıkça büyüme hızı artar. Dolayısıyla, genel olarak değerlendirildiğinde benign tümörler malign tümörlere göre, yıllarla ölçülebilen çok daha yavaş büyüme hızına sahiptir. Ancak, bazı benign tümörler malign tümörlere göre daha hızlı büyüyebilir. Hormonal faktörler ve vasküler beslenme durumu benign tümörlerin büyüme hızını etkileyen faktörler arasındadır. Örneğin, leiomyomlar düz kas dokusundan köken alan benign kas tümörleridir ve uterusta yerleşenler hamilelikte hızla büyüyebilirken, menapozda atrofiye uğrayıp küçülebilirler. Bu durum, kısmen östrojene bağımlı olarak ortaya çıkmaktadır.
Öte yandan nadir de olsa malign tümörlerin de küçülebildiği ve çok nadiren ortadan kayboldukları saptanmıştır.
3. LOKAL İNVAZYON
Benign tümörlerin hemen hemen hepsi, çevre dokulara invazyon göstermeden, sadece çevresindeki normal dokulara bası yapıp, iterek “ekspansif” şekilde, yavaş büyüyen tümörlerdir. Genellikle, çevrelerindeki dokunun stromasından kaynaklanan fibröz bir “kapsül” benign tümörleri çevrelediğinden, çevre dokulardan keskin sınırlarla ayrılır ve kolaylıkla çıkarılabilirler. Hemanjiom, benign bir vasküler tümör olmasına karşın bu duruma bir istisna oluşturur.
Malign tümörler ise çevre dokulara invazyon göstererek, harabiyete yol açarlar. Genel olarak, çevre dokulardan keskin sınırlarla ayrılmazlar. Bazen tümör malign olduğu halde büyüme hızı yavaş ise aynen benign tümörlerde olduğu gibi çevresinde fibröz bir kapsül oluşabilir. Ancak, böyle bir kapsül varlığına rağmen, mikroskopik olarak tümörün genellikle bu kapsülü aştığı ve çevre dokulara invazyon gösterdiği saptanır. Bu nedenle, bu kapsül gerçek değil yalancı kapsüldür ve “psödokapsül” olarak adlandırılır. Malign tümörler anatomik sınır tanımaz ve çevrelerindeki, normal doku stroması dışında lenfatik, damar ve sinir çevresi dokulara da infiltre olurlar. Bu nedenle cerrahi yolla tedavi edilirken, çevrelerindeki belirli bir miktar normak doku ile birlikte çıkarılmaları gerekir.
Bazı malign tümörler, invazyon göstermeden önce bir “invazyon öncesi (preinvaziv)”dönem gösterirler. Bu aşamada, hücrelerde “atipi” kriterleri mevcuttur ancak invazyon izlenmez. Bu durum “displazi” olarak tariflenir ve mikroskopik bir terimdir. Daha çok epitel dokularında görülür. Epitelin bazal membranını aşmamış ve henüz invazyon gösterme yeteneği kazanmamış atipik epitel hücrelerinden oluşan lezyon, belli kriterlere göre “hafif-orta-şiddetli displazi” olarak isimlendirilir. Epitelin tüm katlarını tutan ancak invazyon göstermeyen ağır displastik değişikliklere “KARSİNOMA İN SİTU” denir.
Malign tümörlerin, çevre dokulara invazyonu dokular arasında farklılıklar göstermektedir. Ancak, malign tümör hücrelerinin invazyon için en çok kullandıkları yol “normal dokuların bağ doku stroması”dır. Bağ dokusu içindeki elastik lifler, kollajen liflere göre invazyona daha dayanıklı gibi gözükmektedir. Bu fark olasılıkla malign tümörlerdeki kollajenazın, elastaza göre daha yüksek oranlı olmasından kaynaklanmaktadır.Ancak, yoğun kollajen içeren tendon, eklem kapsülü ve membranlar da uzun süre invazyona dayanıklılık gösterir. Arter duvarının daha sert oluşu yanında, elastin içeriği ve proteaz inhibitörlerini salgılaması nedeni ile arterler venlere göre invazyona daha dirençlidir.
Lokal invazyon metastazdan sonra en önemli malignite kriteridir.
4. METASTAZ
Metastaz kelime anlamı olarak “primer tümör ile devamlılık göstermeyen” tümör odaklarının bulunmasını ifade eder. Bir tümörün malign nitelikte olduğunun EN KESİN kriteridir. Yani, bir tümör metastaz yapmış ise o tümörün kesinlikle malign olduğu kabul edilir. Beyin gliomlarında ve derinin bazal hücreli karsinomlarında çok nadir olmakla birlikte tüm malign tümörler metastaz yapabilir.
Genel olarak, bir tümör ne kadar büyükse ve ne kadar hızlı büyüyor ise metastaz yapma olasılığı o kadar yüksektir. Ancak, bu kuralın istisnaları da vardır.
Metastaz yolları:
1-Vücut boşlukları ve yüzeylerine yayılım: Peritoneal, pleural ve perikardiyal yayılım. En sık over kanserlerinde, appendiks müsinöz karsinomlarında peritoneal tutulum (peritonitis karsinomatoza-psödomikzoma peritonei).
2- Lenfatik yayılım.Daha çok karsinomlarda görülür ama sarkomlarda daha nadir de olsa bu yolu kullanırlar.Tümörlerin kendi lenfatikleri yoktur. Çevre normal dokunun lenfatiklerini kullanarak yayılırlar ve bu nedenle öncelikle bölgesel lenf nodlarına yayılırlar. Genellikle lenfatik drenaj yolunu izlerler ama bazen atlayan (skip) metastazlar görülür.Venöz sistemle olan geçişler, geçirilen inflamasyon ve radyasyona bağlı fibrozis sonucu drene olduğu ilk lenf nodu elverişsiz olunca daha sonraki lenf nodunda tümör yerleşimi olabilir.
Sentinel lenf nodu ise drenaj üzerindeki ilk lenf nodudur ve özellikle meme, kolon kanserleri ile maliğn melanomlarda lenfatik disseksiyon yapılıp yapılmama kararı verilmesinde belirleyicidir.
3- Hematojen yayılım: Sarkomlarda sık yayılım yolu ama karsinomların ileri evresinde e ortaya çıkar. Venler arterlerden daha kolay invazyona uğrarlar. En sık metastaza uğrayan organlar; akciğer (v. kava aracılığı ile) ve karaciğer ( v. porta aracılığı ile) dir.
Bazı kanserlerin özellikle ven invazyonu yapma eğilimi vardır. Böbreğin renal hücreli karsinomu ile karaciğer kanseri (hepatosellüler Ca) erken dönemde ven invazyonu yapan tümörlerdir. Renal hücreli karsinom hücreleri, renal vene ve oradan vena cava inferiora uzanır. Bu yolla sağ kalbe kadar uzanan olgular bile mevcuttur.
Tümörlerin anatomik yerleşimleri ve geliştikleri organların doğal venöz drenajı metastazları tam olarak açıklamak için yeterli değildir. Örneğin prostat karsinomları özellikle lumbar vertebralara, nöroblastom özellikle karaciğer ve kemiklere, akciğer kasrinomları da özellikle adrenal bezlere ve beyine yüksek oranda metastaz yaparlar.